鉛電池を調べました。
負極に海綿状鉛、正極に二酸化鉛、電解液に希硫酸を用いた二次電池です。
自動車、バイク、フォークリフト、ゴルフカート 等用として最も生産量が多い電池です。
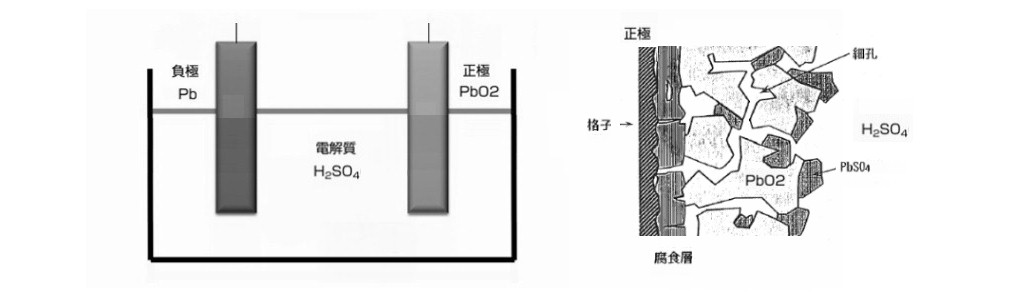
負極の海綿状鉛は、微細構造で表面積を増やしています。
正極の二酸化鉛は、0.1ー1µm の細孔からなる多孔体で、金属酸化物ですが電気伝導性を有しています。
正 負 極の活物質は格子と呼ばれる合金製の集電体に保持されています。
反応式

・放電時は電解液中の硫酸イオンが硫酸鉛となり正極 ・負極に付着します。
・充電時は正極・負極に付着した硫酸鉛から硫酸イオンが電解液中に移動し、負極で鉛、正極で二酸化鉛になります。
特徴
・電極材料の鉛、電解液が安価です。
・短時間の大電流放電、長時間の小電流放電に対応できます。
・メモリー効果がありません。
・高速充電が不可のため、充電時間が長くなります。(充電電流は定格放電電流の1/10以下になります。)
定電圧定電流充電例 (14.8V 10A )

・公称電圧は2Vと比較的高い。
(硫酸電解液を使用することにより、水の理論分解電位を超えています。)
電池電圧の近似試算

硫酸電解液中における電極電位 vs.SHE
二酸化鉛 : 1.8V
鉛 : - 0.38V
劣化
・充放電サイクルにより活物質の微細構造の変化、物性変化が生じる。
・正極板格子は陽極酸化により腐食し、活物質の脱落や電圧低下が起こる。
・過放電状態で放置すると、負極板表面に不導通の硫酸鉛結晶が生じ、電極の表面積が低下し容量が低下する。(サルフェーション)
白動車用鉛電池の重負荷寿命は300-500回です。
関連: